2020/06/01
要旨
- 世界的な新型コロナウイルスの感染拡大にともない、様々な医療物資が不足した。多くの国において、正式な輸出禁止や制限が課される事態に発展した。
- 日本も含め、国内での医療資源の増産を進める動きが活発化した。しかしながら、人工呼吸器をはじめとする医療機器の増産は、メーカーにとって、多くの課題がある。
- 数多ある医療機器の中から、集中治療室に必要な医療機器を見てみると、これらの国内生産比率は、多くの製品分野で50%を下回っており、平常時においても低い状況となっている。
- 短期的な対応策としては、制度の見直しや異業種企業の支援といった人海戦術が中心となる。中期的な対応策としては、スマートなマザー工場によってスケールアウトできる仕組み、あるいは自動車業界をはじめとする輸送機器産業において先行する、Industry4.0の取り組みを医療機器に応用することができれば需要に合わせてバーチャルな増産体制を組むこともできると考える。いずれも医療機器メーカー単独での対応は難しく、異業種企業と公的機関をまじえながら、産業大で取り組む必要がある。
世界的に医療機器が不足。医療機器の輸出制限も発動
2020年5月19日現在、新型コロナウイルスの治療薬、あるいは有効な治療方法は確立されていない。国内における新型コロナウイルス感染症対策専門家会議は、「アフリカなどではこれからもまん延が継続する可能性がある。こうした世界的な動向や国内における感染状況を見据えると、今後とも、一定期間は、この新たなウイルスとともに社会で生きていかなければならないことが見込まれる」(2020年5月1日発表)としており、感染拡大に対する備えが、今後も継続して重要となっている。
WHOは、2020年3月11日に、新型コロナウイルスを世界的なパンデミックと宣言した。このころから、各種の医療用機器・資材の不足が顕著となってきた。まず、イタリア、スペイン、米国等の欧米各国において、感染の有無を同定するための検査キットや、検査の際の飛沫感染リスクを抑制するための医療用フェイスシールドや医療用マスク、医療用防護服といった消耗品が不足した。そして、感染者の中から、重症の患者が増加すると、人工呼吸器や人工肺といった医療機器も不足するようになった。
このような状況下において、各国政府による、国外への輸出制限が発動される事態に陥った。以下に例を挙げる。
- 米国政府は、合衆国輸出入銀行(U.S. EXIM Bank)による、人工呼吸器をはじめとする特定の医療機器や医療用具の輸出に対する資金援助を凍結
- ドイツ当局が、スイスの販売事業者による医療用マスクの輸送を停止
- フランス政府が、国内メーカーによる英国への販売契約を停止
- インド政府は、人工呼吸器、検査キットの輸出を禁止 など
このような正式な輸出禁止、あるいは事実上の輸出禁止や制限を課した国は、欧米諸国を中心に、20か国以上に及ぶ。
各国政府による増産の指示や呼びかけが相次ぐも、医療機器の増産実現はハードルが高い
2020年4月7日、日本政府は緊急経済対策を発表し、人工呼吸器、人工肺装置、医療用マスク、医療用ガウンを対象とする増産の呼びかけを行った。これに伴い、経済産業省は、「人工呼吸器生産のための設備整備事業」にもとづく公募を行った。また、医療用マスクやガウンをはじめ、フェイスシールドや消毒用品などの消耗品は、異業種の企業による製造が日を追って進められた。しかし、人工呼吸器をはじめとする医療機器は、人工呼吸器メーカーである日本光電が増産に取り組んだり、一部の部品を異業種の企業が製造し始めたりしているものの、依然として増産実現のハードルは高い。
日本の動きに先行した米国、英国の政府は、より大規模な事業を展開してきた。英国は、人工呼吸器1万台を増産するために、約30社で組織するコンソーシアム「Ventilator Challenge UK」がサプライチェーンの構築を進める。同コンソーシアムでは、ロールスロイス社が計測器、バルブ、ポンプを、GKNエアロスペース社が組み立てを、シーメンス・メディカル社が品質の管理を行うなどの分業体制が敷かれた。米国は、連邦政府による国防生産法のもと、人工呼吸器の製造の指示を受けたフォード・モーター社が、GEヘルスケア社と提携し、月間3万台の人工呼吸器の製造ラインを構築。ゼネラルモーターズ社は同様に、米国の人工呼吸器メーカーであるベンテック・ライフ・システムズ社と生産業務において提携し、人工呼吸器を製造した。
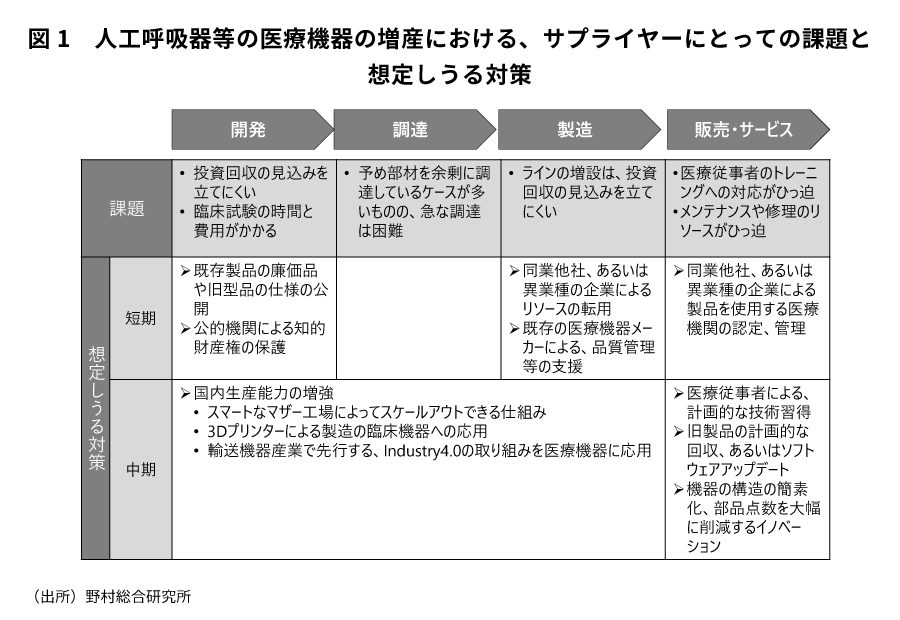
国内では、4月に経済産業省による「人工呼吸器生産のための設備整備事業」の公募事業が開始されたが、目標としていた数量の実現には至っていない。供給者は、様々な課題を抱えている(図1)。
まず、既存の医療機器メーカーが製造ラインを増設することが期待されるが、平常時の医療機器の需要は、それほど大きく変動するものではないため、パンデミックが収束した後も含めた長期的な投資回収の見込みを立てにくい。このことが、既存の医療機器メーカーが最も頭を抱える課題であり、自社単独での解決策を見出しにくい。この課題を解決する手段として、米国政府が主導する、自動車メーカー等の異業種の企業が既に保有する製造リソースを転用し、最終組み立てなどの製造業務の一部を担うことは理にかなっている。この場合、英国におけるシーメンス・メディカル社や米国におけるGEヘルスケア社が担っているような、既存の医療機器メーカーによる品質管理などの支援は欠かすことが出来ない。
また、異業種の企業が、にわかに医療機器の新製品を開発するには、開発投資の回収や開発期間の長期化が課題となる。この課題に対しては、既存の医療機器の廉価品や旧型品といった、医療機器メーカーにとって収益貢献の低い機種について、製品の仕様情報を公開するといった大胆な対策も想定しうるが、この場合、医療機器メーカーが一方的な損害を被ることがないよう、公的機関が知的財産権を保護することが必要となる。
さらに、異業種の企業が製造に関与した医療機器の利用環境・利用条件も重要な要素となる。使用する医療機関側が技術に習熟し、正しく使用されることが担保されないことには、たとえ、医療機器メーカー側が品質管理を担うとしても、異業種の企業にとっては依然として大きなリスクを感じる。これに対しては、米国国防生産法においては、異業種の企業が製造した医療機器に特例的な承認を与える一方で、医療機器を使用する医療機関側に対しても、当局が認定をし、管理するという対応がとられている。
これらは、いずれも既存の法規制に対して特例的な措置をとることを決定するといった点で、短期的な対応策として想定しうる。しかしながら、日本においては、安価な製造コストを求めて国外に生産拠点を移したり、あるいは外国メーカー製品の輸入に依存するといった手段を選択してきた結果として、医療機器の国内供給力が低いことが、かねてより問題視されてきた。
集中治療室に必要な医療機器の多くが、国内供給力が極めて低い
新型コロナウイルスに関しては、2020年4月の緊急事態宣言が解除されたとしても、日本において、感染者数増加の新たな波が訪れる可能性は残る。諸外国では、新たな波に備えた対策に着手する動きも報じられている。さらに、近年、感染症のパンデミックが続いていることから、日本も、抜本的な対策を検討すべきと考える。
日本集中治療医学会は、同学会の危機管理委員会において、「インフルエンザ大流行や大災害時の集中治療室と病院における対策のための推奨手順と標準手順書」をとりまとめ、提言している。集中治療室に必要な医療機器として、以下が挙げられている。
- 人工呼吸器
- バッグバルブマスク(手動で人工呼吸を行うための機器、蘇生バッグ)
- ネブライザー(薬剤を含んだ細かい霧を発生させる機器)
- 吸引器
- 心拍数、血圧、呼吸、心電図のモニター
- 非観血的血圧計
- パルスオキシメーター(血液中の酸素飽和度と脈拍数を測定する機器)
- 血液透析および血液濾過装置
- 輸液ポンプ、経腸栄養用ポンプ
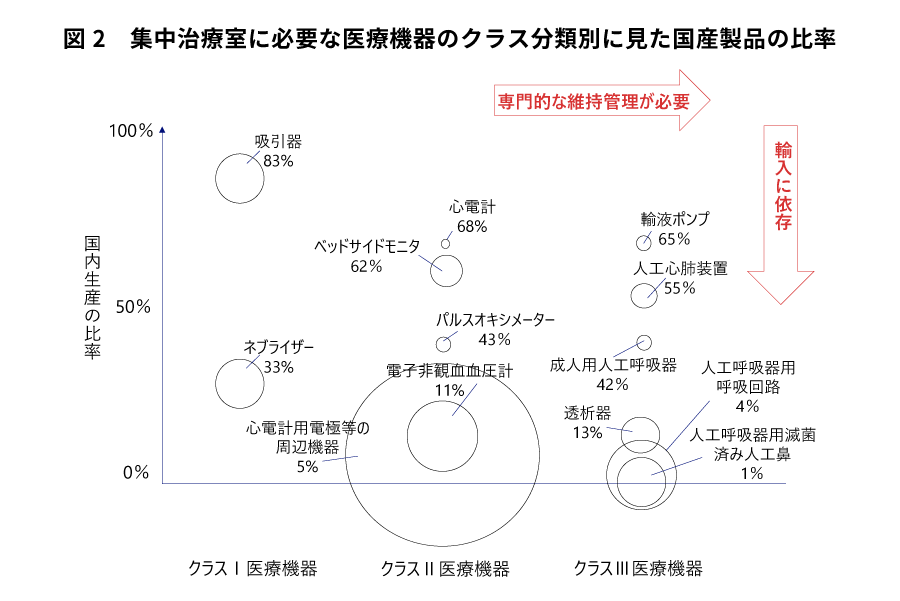
しかしながら、日本は、これらの医療機器を自国で十分に供給することが難しい状況にある。図2は、集中治療室に必要な医療機器の国内生産の比率を示す。医療機器としての高度な管理を必要としないクラスⅠの吸引器は、国内生産の比率が83%であり、他の医療機器と比べて最も高い。次いで、心電計68%、輸液ポンプ65%と続くが、いずれも70%を下回る。
なかでも、クラスⅢの人工呼吸器用滅菌済み人工鼻は1%、人工呼吸器用呼吸回路は4%であり、国内生産の比率が極めて低い。これらの機器は、新型コロナウイルスで問題視されている人工呼吸器に接続して使用する消耗品である。人工呼吸回路の多くは各接続部が容易に外れやすいスリップイン式であり、人工呼吸回路由来の医療事故は、厚生労働省の医療事故情報収集事業へのヒヤリハット報告が毎年100件近く為されてきた。日本臨床工学技士会 がかねてより警鐘を鳴らすが、国外のメーカーにより設計、製造されていることから、抜本的な解決が難しいとされていた。
また、クラスⅢの医療機器は、医療従事者が適切に使用するための技術を習得するために、医療機器メーカー(あるいは販売代理店)によるサポートを必要とするケースが多い。また、医療機関への導入後、継続的なメンテナンスや修理を必要とし、それらを医療機器メーカーが管理している。すなわち、これらの活動に必要な情報が、日本国内では十分に確保できないことを意味している。
このように、従来から医療機器が抱えていた問題が、新型コロナウイルスをきっかけとして浮き彫りになった形であり、いよいよ解決が求められる。
-
(出所)
日本集中治療医学会「インフルエンザ大流行や大災害時の集中治療室と病院における対策のための推奨手順と標準手順書」、厚生労働省「平成30年薬事工業生産動態統計年報統計表」をもとに野村総合研究所作成
-
注)
円の大きさは、吸引器の国内消費量(数量)を100とした場合の相対的な量を表した。
-
注)
医療機器4000を超える種類が存在し、「医薬品、医療機器等の品質、有効性及び安全性の確保等に関する法律(薬機法)」によって、その使用における安全上のリスクや用途などにより、4つに分類されている。「クラスⅠ」は、一般医療機器と呼ばれ、不具合が生じても身体への影響が極めて小さいと考えられる機器。「クラスⅡ」は、管理医療機器と呼ばれ、身体への影響が比較的小さいと考えられる機器。「クラスⅢ」は、高度管理医療機器と呼ばれ、身体への影響が比較的大きいと考えられる機器。ちなみに、「クラスⅣ」は、患者への侵襲度が高く、不具合が生じた場合に生命の危険に直結するおそれがあると考えられる機器。
既存の医療機器メーカー単独での生産能力の増強には限界があり、企業間のバーチャルな共創システムの構築に、産業大で取り組むべき
既に述べた通り、増強策を既存の日系医療機器メーカーのみで実行することは、投資回収の観点から現実的ではない。また、日本においては、医療機器メーカーの80%以上が中小企業で占められていることからも、急な需要の拡大に対して個々の医療機器メーカーが単独で応じることは、容易ではない。
そのため、急激な需要拡大が見込まれる際に、異業種の企業を含めた複数の企業がバーチャルに集積して、必要な医療機器を生産できる体制を構築すべきである。体制の構築にあたっては、感染症のパンデミックの度に、政府と行政が新たに企業に呼び掛けるのではなく、図2に示した集中治療室に必要な一連の医療機器については、必要に応じて柔軟に集合し、集中的に生産し、供給することができるようなコンソーシアムをつくっておくべきであろう。
コンソーシアムは、図1に示した「想定しうる対応策」の「短期」に示した項目について、参加企業と行政が連携し、具体化を検討するところから着手されたい。また、コンソーシアムは、医療機器の業界団体が担うことによって産業大の取り組みにすることができないだろうか。そうすることによって、特定の医療機器に偏ることが無く、多様な医療機器メーカーの参加を募りやすくなるのではないか。なお、同連合会は、医療機器メーカー以外の異業種企業の参画も可能な仕組みになっている。さらに、この仕組みを具体化する過程において、近年、国が整備してきた国立研究開発法人日本医療研究開発機構(AMED)が有する、医薬品医療機器総合機構(PMDA)と企業との連携支援機能も有望とみる。
医療機器産業では成功事例がみられないが、半導体露光装置メーカーが、スマートなマザー工場によってスケールアウトできる仕組みを構築した成功事例が参考になる。これは、オランダの半導体製造装置メーカーASML社の事例が有名だが、同社が2000年代に、当時牙城だったキヤノンとニコンに挑んだ手法である。同社は、製品を構成する機能ごとに、外部のメーカーも参加できるモジュラー構造を開発設計に取り入れた。このことによって、同社は、顧客の要望に対して、競合よりも低コスト、かつ柔軟に応じることに成功した(詳細は、野村総合研究所「第4次産業革命に流れる本質」(知的資産創造2019年9月号)を参照)。
また、自動車業界をはじめとする輸送機器産業において先行する、Industry4.0の取り組みにも学ぶところが大きいと考える。これは、ドイツをはじめ、日本、中国、インドなどで戦略的に進められている。例えば、製造プロセスと手順をデジタル化したりオートメーション化したりすることにより、企業の垣根を超えて製造工程に複数の企業が参画することを可能にする仕組みを構築している。そのために、設計段階から、製造工程にシームレスに設計データが統合され、仮想的な製造拠点の構築を可能にする仕組みとなっている。この仕組みを機能させるうえで、部品の製造受託メーカーが、3Dプリンターを用いて試作品を作成する取り組みもなされている。今後3Dプリンターの開発が進み、医療機器においても応用することができれば、この仕組みの上で、需要に合わせてバーチャルな増産体制を組むこともできるのではないか。医療機器産業の場合は、極めて多岐にわたる種類の機器が、多岐にわたる部品や材料によって成り立っていることから、特定の企業が単独で仕組みを構築するよりも、産業大で仕組みを構築する方が効率的であり、得られる成果も大きいことも、前提として考慮されるべきである。
執筆者
松尾 未亜
グローバル製造業コンサルティング部
お問い合わせ先
報道関係者からのお問い合わせ
-
株式会社野村総合研究所 コーポレートコミュニケーション部
提言内容に関するお問い合わせ
-
株式会社野村総合研究所 未来創発センター